无锡耐思生命科技股份有限公司品牌商
10 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
推荐产品
公司新闻/正文
喜报喜报|耐思重复笔通过欧盟MDR认证!
19 人阅读发布时间:2026-04-23 08:59
在全球医疗器械监管持续趋严的大背景下,合规能力正逐渐成为企业参与国际竞争的“入场券”。近日,耐思重复笔成功通过欧盟MDR认证,标志着公司在高端医疗器械领域的质量体系与产品性能,已全面达到国际严苛标准。



欧盟医疗器械法规——Medical Device Regulation (MDR),于2021年正式全面实施,取代原有的MDD指令,被认为是全球最严格的医疗器械监管体系之一。
相较于旧规,MDR在多个维度显著升级:
- 临床评价要求更高:强调真实临床数据支撑
- 全生命周期监管:从设计、生产到上市后追踪全面覆盖
- 可追溯性强化(UDI系统):确保产品全流程透明
- 技术文档要求严苛:对风险管理与性能验证提出更高标准
可以说,MDR不仅是法规升级,更代表着全球医疗器械行业向高质量、安全性、可追溯性全面跃迁。
👉通过MDR认证代表着:
-
拥有进入欧盟市场的“通行证” -
产品质量与安全性获得国际权威认可 -
企业质量管理体系达到全球领xian水平 
- 成功通过MDR认证,意味着什么?
此次耐思重复笔顺利通过MDR认证,核心意义主要体现在三个层面:
-
产品力:达到国际高标准
重复笔作为药物递送系统的重要组成,对剂量精准性、结构稳定性、使用安全性要求极高。通过MDR认证,意味着耐思产品在设计验证、性能测试及风险控制方面,已达到欧洲市场的高门槛。
-
体系力:质量管理全面升级
MDR不仅审核产品,更审核企业体系。耐思在质量管理、生产控制及文件体系上的全面优化,确保产品从研发到交付的每一环都可控、可追溯。
市场力:全球化布局加速
获得MDR认证后,耐思将具备更强的国际市场拓展能力,在欧洲及其他高端市场的竞争中占据主动。
取得MDR认证的前提
获得Medical Device Regulation (MDR)认证,并非单一测试通过,而是建立在数据充分、风险可控、体系闭环的系统性验证基础之上。
1.产品验证与性能确认
企业需提供充分证据证明产品的安全性与有效性,主要包括:
设计验证:确保产品符合既定技术要求
性能测试:如剂量准确性、耐久性、稳定性
生物相容性评估:符合ISO 10993系列标准
可用性工程:验证临床使用安全
对于重复笔类产品,还需重点验证多次使用稳定性与长期可靠性。
2.临床评价要求
必须基于临床数据开展评价,包括文献分析、临床试验或等效数据,并实施上市后临床跟踪(PMCF),对数据能力要求显著提升。
3.全生命周期质量体系企业需建立符合国际标准的质量体系(通常基于ISO 13485),并满足MDR附加要求:风险管理体系(ISO 14971)
生产过程控制与验证
供应链可追溯管理
上市后监督(PMS9)与不良事件报告
MDR强调:产品合规不是阶段性,而是贯穿整个生命周期的持续过程
4.技术文档与可追溯性需提交完整技术文件,并满足UDI及EUDAMED注册要求,确保产品全流程可追溯。认证过程中需提交完整技术文档,并满足UDI(唯1器械标识)等要求:
技术文件完整性
风险-收益分析报告
标签与说明书合规性
UDI编码与数据库注册
任何环节不达标,都可能导致审核延迟甚至失败。5. 审核难度与行业现状
MDR实施后审核周期延长至12–24个月,审核资源紧张,大量企业被淘汰,行业普遍认为,MDR认证已从“合规要求”升级为高门槛筛选机制。
总结来看,通过MDR不仅是合规要求,更是企业综合实力与国际竞争力的体现。
从重复笔到药包材:耐思的整体布局优势
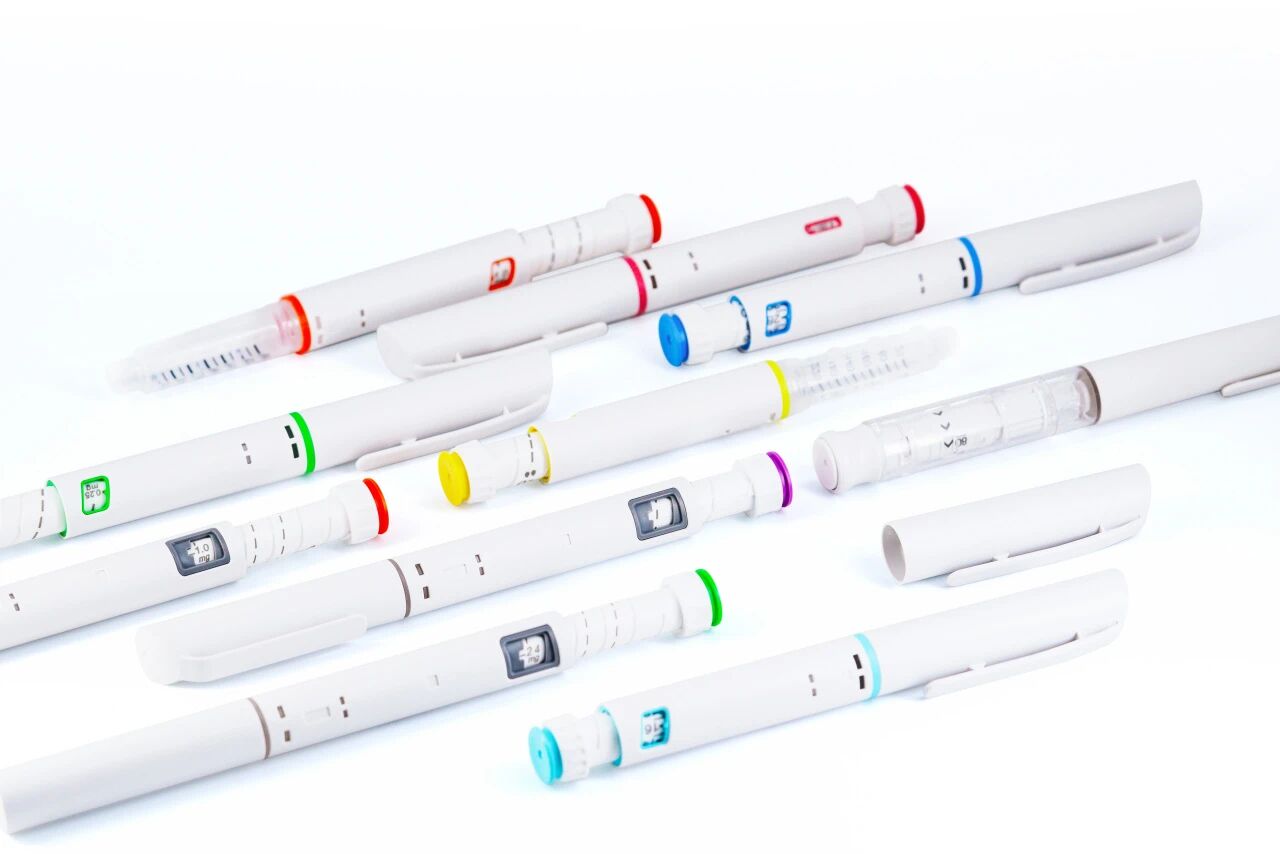
耐思目前已推出了可重复使用的笔式注射器、更经济的一次性笔式注射器(常规款、SP款、内旋式笔、自动注射笔等)为生物制药行业提供更安全、更便捷、更人性化的自我给药解决方案。
可广泛应用于司美格鲁肽、促卵泡素(FSH)、利拉鲁肽、胰岛素、生长激素等相关药物。
产品优势:
产品规格多样化
精准的注塑工艺,产品的一致性高产品验证与专利风险规避高度可定制化服务 -
-

新型药用包装材料
-
√ CDE登记号
√ MDSAP五国体系认证
√ 510(k)NO.K240961
√ DMF NO.40744
√ 中美FTO审查,无专利风险
√ MDL NO. 113733
√ PB-UMKU: 051223002876400010018
-
RTU卡式瓶
-

√ 免洗免灭
√ 湿热灭菌
√ 硅化处理,烘烤固化
MDR认证的通过,并非终点,而是耐思迈向更高标准的开始。 在全球医药产业持续升级的趋势下,合规能力+产品创新+制造实力将成为企业长期竞争的核心。耐思正通过持续投入与技术积累,稳步构建自身在高端药包材与给药系统领域的全球竞争力。 未来,随着更多产品完成国际认证,耐思有望在全球舞台上占据更加重要的位置。





