无锡耐思生命科技股份有限公司品牌商
10 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
推荐产品
公司新闻/正文
双令落地,耐思构建实验耗材安全体系新标准
14 人阅读发布时间:2026-05-11 16:08
2026年5月,随着国务院令第818号与第828号正式施行,中国细胞治疗产业将从高速发展迈入规范化、体系化的新阶段。监管逻辑正从“鼓励创新”转向“创新与安全并重”,并由局部规范升级为系统治理,本质上是在重塑行业基础标准。
从政策层面看:
-
818号令(生产端):强化GMP与全过程质量控制,强调生产必须“可控”
-
828号令(监管端):完善全生命周期监管与追溯体系,强调产品必须“可查”
在此背景下,实验室耗材的角色被重新定义:
-
准入门槛提升,低标准产品将被淘汰
-
验证要求前移,上游需提供生物相容性及可提取物等数据
-
数据完整性增强,批次必须可追溯
-
审计压力向供应链延伸
总体来看,双令将推动行业从“制造导向”转向“质量体系导向”,并加速向高标准、高验证与高合规方向集中。


一、NEST TriSteriTM超低微粒产品
在强监管与高标准并行的背景下,针对细胞治疗、基因治疗等对洁净度要求极高的应用场景,耐思推出 TriSteriTM超低微粒系列产品,为高端生物制药与前沿科研提供更可靠的耗材解决方案。
应用场景适配(覆盖GMP核心环节)
-
适用于大规模细胞培养、原液无菌分装、API取样、制剂灌装等关键流程
-
支持关键试剂转运等高洁净要求操作
-
满足细胞治疗、基因治疗等高端应用场景需求
产品优势:
-
超低微粒控制
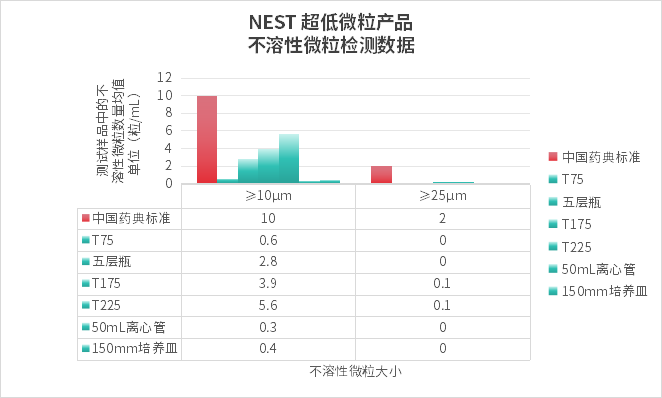
每批产品均参照中国药典采用光阻法进行不溶性微粒检测。
检测结果:不溶性微粒含量远低于中国药典限值,从源头降低污染风险,保障细胞状态与产品稳定性。
严格产品质检
所有产品均进行2次外观检测,确保流出的每一个产品均无可视异物。

(每款产品的最小包装均有批号标记,方便产品的质量查询。)
-
体系认证
无菌水平达SAL=10-6,无DNase/RNase,无内毒素,无细胞毒性。符合 ISO 13485(医疗器械质量管理体系)和 ISO 9001认证。
-
三层包装与洁净防护
符合GMP标准的三层包装体系,有效阻隔外界污染物进入洁净区,提升无菌环境下操作安全性
-
质量验证与合规支撑
通过系统性检测与验证,满足生物药生产与科研实验对高质量与数据准确性的双重要求 -


二、实验室耗材的“硬门槛”
结合政策导向与行业实践,实验室耗材需要满足的不再是单一性能指标,而是一个系统性能力集合
-
原材料安全性(低风险输入)
-
生产过程控制(GMP级输出)
-
无菌保障能力(可量化指标)
-
数据与文件完整性(审计支撑)
而这四点,正是当前多数企业面临的短板,也是行业洗牌的关键分水岭。
01 高品质原材料体系
耐思均选用符合USP Class VI标准的医用级原材料,确保成分明确、化学性能稳定且不含任何动物源成分
从源头降低:
-
细胞毒性风险
-
可提取物干扰
-
实验波动性
实现:输入即高标准

02 GMP洁净制造 + 高自动化生产
耐思生产体系具备:
-
GMP标准洁净车间
十万级洁净车间10600m2,万级洁净车间3600m2,注射笔管控车间2300m2,预灌封成型管控车间850m2
-
高自动化成型与装配设备
引进国际先进ASB注拉吹塑设备
-
标准化生产流程控制
原料采购-生产-包装-灭菌-交付
核心价值在于:
-
降低人为污染变量
-
提高批次一致性
-
确保规模化稳定输出
在监管语境下:制造过程本身就是质量证明的一部分



03 无菌保障体系
耐思园区自有灭菌中心-福腾辐照灭菌中心。
灭菌中心面积超过8000平方米,先后引进国际领xian的比利时 IBA Rhodotron® TT300 、Rhodotron' TT200 双射线加速器,实现从物料流转到辐照实施的全链路精准控制。
-
SAL(无菌保障水平)10⁻⁶
-
高效穿透、稳定灭菌
-
满足美国FDA要求
这不仅是技术指标,更是风险概率的量化控制能力


04 第三方验证体系
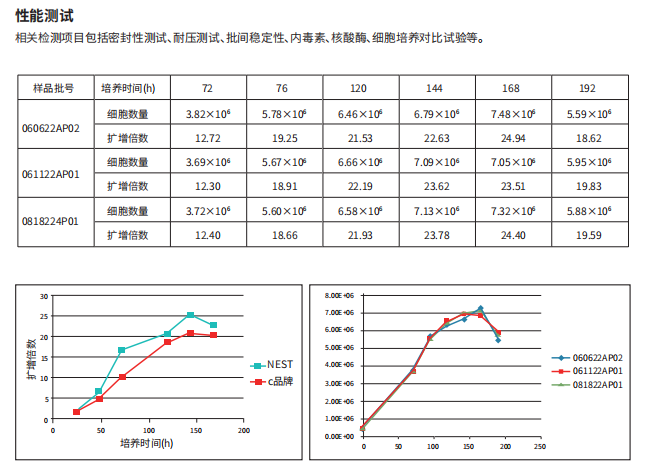
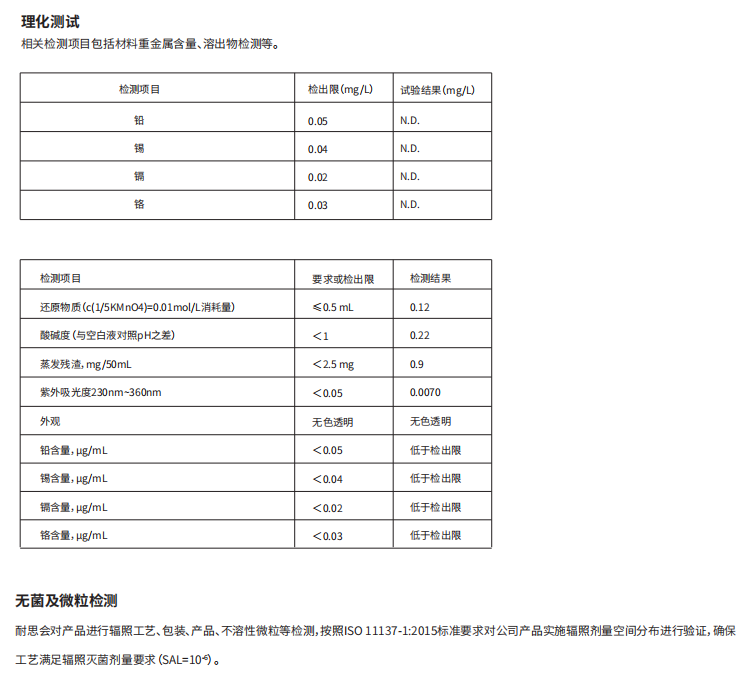
耐思对产品开展系统性验证:
-
生物相容性测试
-
细胞毒性评估
-
可提取物/浸出物研究
输出:
-
完整验证报告
-
审计支持文件
-
合规备案资料
实现:从“宣称安全”到“证明安全”
05 全生命周期追溯
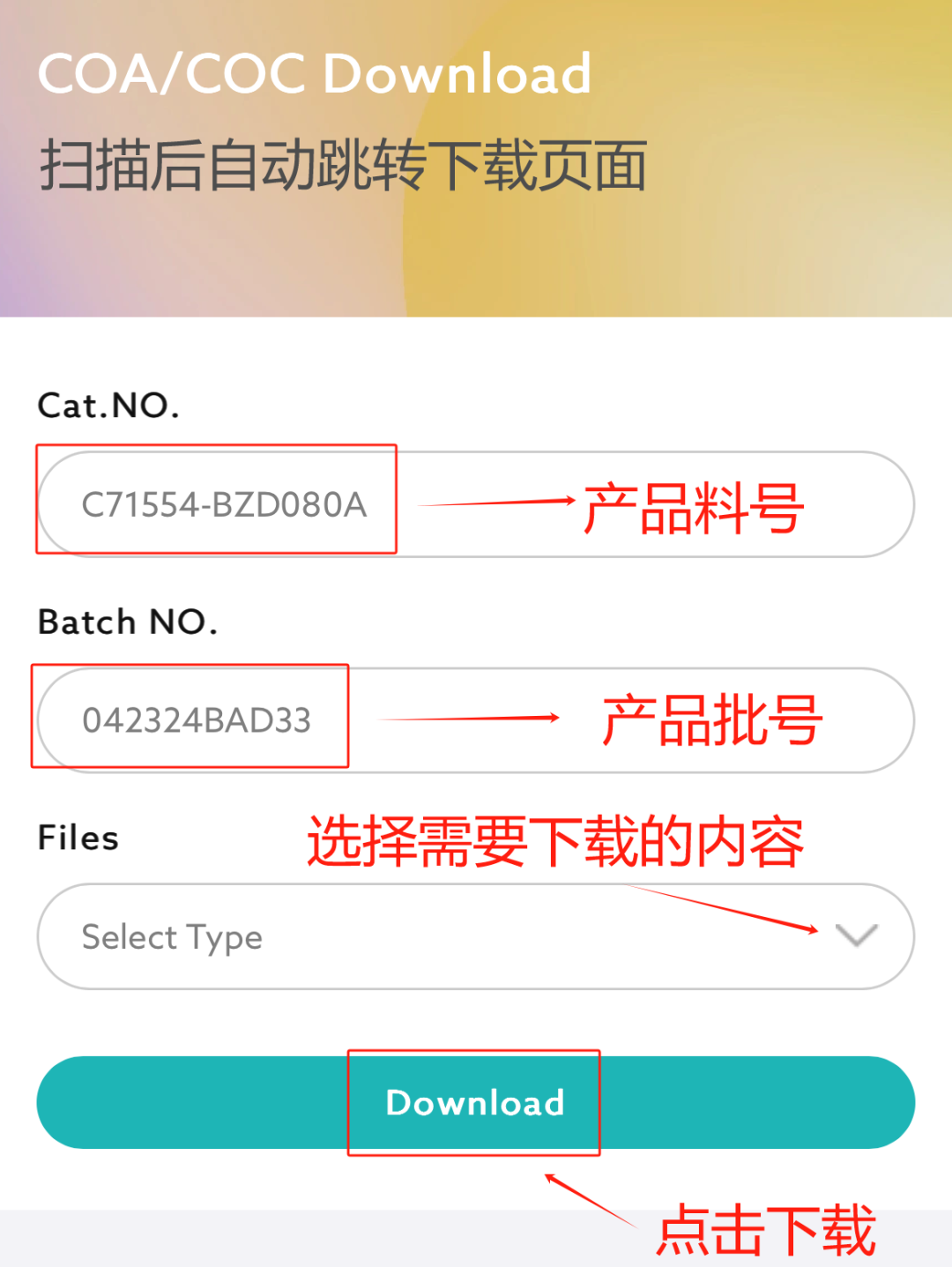
耐思全面升级包装与数据体系:
-
COA二维码集成
-
一键获取COA / COC
-
批次信息可追溯
满足:
-
审计需求
-
合规核查
-
客户质量管理体系对接
实现:产品即数据入口

三、全产品线协同

无锡耐思十余年来深耕生命科学行业,不断拓宽产业线,从最初的实验室耗材,到如今医疗器械、新型药用包装耗材、生物样本库解决方案、生物工艺配件等,始终秉持着“做高端耗材,创国际知名品牌”的信念、坚持着以自主创新作为蓬勃发展的主推手。
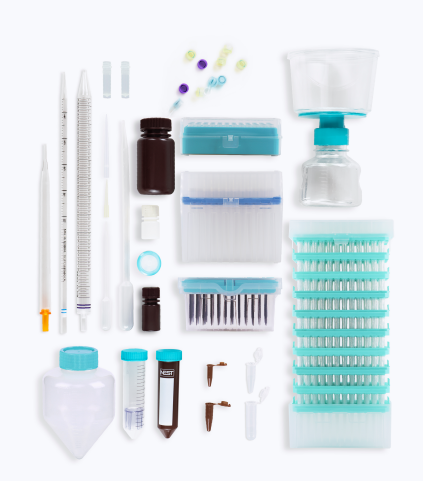
01 实验室耗材
细胞学类耗材、微生物检测类耗材、分子生物学类耗材、生物工艺类耗材
NEST实验室耗材种类丰富,采用高品质原料,以超精密模具和全自动化生产工艺生产,确保无菌、无热原、无细胞毒性。规格种类齐全,可以满足各种实验需求。为细胞培养提供安全、高效的全程保障。


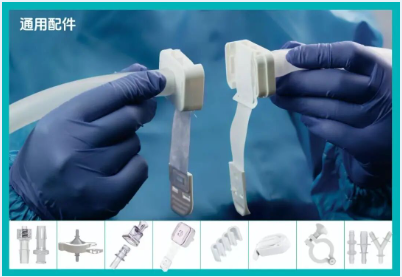
02 医药包装耗材
一次性使用笔式注射器、预灌封自动注射器、内旋式笔式注射器、可重复使用笔式注射器、免洗免灭系列

818号与828号的实施,本质上不是限制行业发展,而是在重建行业信任机制。
未来,企业之间的差距,将不再体现在“是否合规”,而体现在:
谁的产品更稳定、谁的体系更完整、谁的数据更可信。耐思将持续以高标准原材料、先进制造体系、严格无菌保障与完整验证能力为基础,构建长期可靠的产品力与质量力。
在不确定的行业环境中,耐思所提供的,是可以被验证的确定性。
-
-






